Bài 2: Kí hiệu nguyên tử biểu lộ đầy đủ đặc thù cho một nguyên tử của một yếu tố hoá học bởi nó mang lại biết
A. Số khối A. C. Nguyên tử khối của nguyên tử.
Bạn đang xem: Giải bài tập hóa 10 trang 14
B. số hiệu nguyên tử z. D. Số khối A với số hiệu nguyên tử z.
Chọn lời giải đúng.
Chọn D số khối A và số hiệu nguyên tử z.
Bài 3: Nguyên tố cacbon bao gồm hai đồng vị :
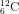
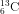
Nguyên tử khối vừa phải của cacbon là :
A. 12,500; B. 12,011 C. 12,022; D.12,055.
Chọn B. Nguyên tử khối mức độ vừa phải của cacbon là: (12 . 98,89 +13 . 1,11)/100 = 12,011
Bài 4: Hãy xác minh diện tích phân tử nhân, số proton, số nơtron, số electron, nguyên tử khối của những nguyên tử thuộc các nguyên tố sau:
73Li ; 199F ; 2412Mg ; 4020Ca
Đáp án bài 4: Ta có: 73Li mang đến ta biết:
Số điện tích hạt nhân là 3, trong hạt nhân gồm 3 proton, không tính vỏ gồm 3 electron.
Số khối là 7, vậy ta có số nơtron là:
N = A- Z = 7- 3 = 4.
Nguyên tử khối là 7 (7u).
Tương từ ta có: 199F gồm Nguyên tử khối là 19 (19u).Số năng lượng điện hạt nhân là 9, trong phân tử nhân gồm 9 proton, ko kể vỏ bao gồm 9 electron.
Số nơtron là 19 – 9 = 10.
2412Mg trongđó:Nguyên tử khồì là 24.
Số năng lượng điện hạt nhân là 12, trong hạt nhân có 12 proton, ko kể vỏ có 12 electron.
Xem thêm: Em Là Cô Gái Hay Mộng Mơ - Cô Gái M52 (Huyr & Tùng Viu)
Sô nơtron là 24 – 12 = 12.
4020Ca trong các số đó :Nguyên tử khối là 40.
Số năng lượng điện hạt nhân là 20, trong hạt nhân có 20 proton, ko kể vỏ có đôi mươi electron.
Số nơtron là: 40 – 20 = 20.
Bài 5 Trang 14 Hóa Đồng gồm hai đồng vị 6529Cu cùng 6329Cu . Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm của mỗi đồng vị.
Giải bài 5: Gọi a là thành phần % của đồng vị 6529Cu; % của đồng vị 6329Cu là 100 – a Ta tất cả :
(a65 + (100-a)63)/100 = 63,54
Giải ra ta được a = 27% 6529Cu. Vậy nguyên tố 6329Cu là 73%.
Bài 6: Hiđro gồm nguyên tử khối là 1,008. Hỏi có bao nhiêu nguyên tử của đồng vị 21H trong 1ml nước (cho rằng trong nước chỉ bao gồm đồng vị21H cùng 11H)? (Cho khối lượng riêng của nước là 1 g/ml).
Giải bài 6:
Gọi % đồng vị 21H là a:
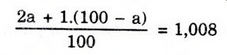
⇒ a = 0,8;
Khối lượng riêng rẽ của nước 1 g/ml, vậy 1ml nước có khối lượng 1g. Khối lượng mol phân tử của nước là 18g.

Bài 7 Oxi tự nhiên là một lếu láo hợp những đồng vị: 99,757% 16O; 0,039% 17O; 0,204% 18O. Tính số nguyên tử của mỗi các loại đồng vị khi có 1 nguyên tử 17O.
Đáp án cùng giải bài 7:
Theo tỉ lệ thành phần đề bài ta có:

Tỉ lệ từng đồng vị O trong các thành phần hỗn hợp 3 đồng vị:
99,757% 16O => 99757 nguyên tử 16O
0,039% 17O => 39 nguyên tử 17O
0,204% 18O => 204 nguyên tử 18O
Khi gồm một nguyên tử 17O thì số nguyên tử:
16O là: 99,757/0,039 = 2558 nguyên tử.
18O là: 0,204/0,039 = 5 nguyên tử.
Vậy trường hợp như có một nguyên tử 17O thì gồm 2558 nguyên tử 16O và bao gồm 5 nguyên tử 18O.
Bài 8: Agon bóc tách ra từ không gian là lếu hợp ba đồng vị : 99,6% 40Ar; 0,063% 38Ar; 0,337% 36Ar. Tính thể tích của 10g Ar ở đk tiêu chuẩn.
Giải bài bác 8:Nguyên tử khối trung bình của argon là:
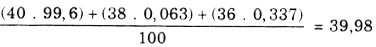
22,4 lít Ar ở đktc có khối lượng 39,98 g
x lít Ar ở đktc có trọng lượng 10 g
Vì nguyên tử Ar tất cả một nguyên tử nên cân nặng mol phân tử của Ar là 39,98 g. Ở đktc thì 1 mol phân tử Ar tốt 39,98g có thể tích là 22,4l. Vậy 10g Ar hoàn toàn có thể tích là 22,4 .10 /39,98 =5,6 (lít)












